#10 روش درمان ناباروری در آقایان و خانم ها

مهمترین تفاوت ایدز با HIV چیست؟ و هرکدام چه علایمی دارند ؟
6 اردیبهشت 1401
پاپ اسمیر چیست و چه افرادی باید این تست را انجام دهند؟
7 اردیبهشت 1401
ناباروری یکی از مشکلاتی است که امروزه در میان زوج های جوان بسیار دیده می شود.
امروزه درمانها و تکنیکهای متنوع و متفاوت زیادی برای درمان مشکلات ناباروری وجود دارد که در ادامه بطور مفصل به توضیح آنها پرداخته ایم.
برای به دست آوردن اطلاعات کافی در مورد ناباروری و روشهای درمان آن لازم است ابتدا بدانید ناباروری چیست و به چه افرادی نابارور گفته
می شود.
بر خلاف باور بسیاری از افراد ناباروری به معنی ناتوانی دائمی در بچه دار شدن نیست.
گاهی ممکن است اختلالاتی در بدن وجود داشته باشد که باعث به وجود آمدن مشکلاتی برای بارداری در خانم و یا آقا شود و با حل این اختلالات
مشکلات مربوط به بارداری به طور کامل حل شود.
ناباروری به این معنی است که زوجین حداقل یک سال رابطه جنسی منظم, بدون اینکه خانم (زیر 35 سال) از داروهای پیشگیری استفاده کرده باشد,داشته باشند و این رابطه منجر به بارداری نشده باشد. لازم به ذکر است مشکلات بارداری فقط مختص خانم ها نیست و ممکن است اختلالات ناباروری از جانب آقا باشد.
علائم ناباروری چیست؟
در صورتیکه بعد از داشتن یکسال رابطه جنسی منظم و بدون استفاده از روشهای جلوگیری از بارداری, باردار نشدید و هر یک از علائم زیر را در خود مشاهده کردید توصیه می شود حتما به متخصص زنان و زایمان مراجعه نمایید.
- تغییر در تمایلات جنسی
- اختلالات پوستی مانند افزایش جوش و آکنه
- ریزش موی شدید یا نازک شدن تارهای مو
- رشد موهای زائد در نواحی قفسه سینه,پشت لب و چانه
- خروج ترشحات شیری رنگ از نوک سینه ها
- احساس درد هنگام رابطه جنسی
- تغییر و بی نظمی در عادت ماهیانه
- افزایش وزن
بررسی علل ناباروری در خانمها

وجود یک سری اختلالات در بدن خانمها منجر به ناباروری و عدم نتیجه تلاش برای بارداری می شود.
در صورت ابتلا به هر یک از این بیماریها لازم است ابتدا جهت بررسی و درمان بیماری اقدام نمایید:
ابتلا سندروم تخمدان پلی کیستیک
مبتلا بودن به این بیماری می تواند یکی از دلایل اختلال در تخمک گذاری باشد.
انسداد لوله های رحمی
انسداد لوله های رحمی مانع از انتقال اسپرم به رحم می شود.
ابتلا به اندومتریوز
اندومتریوز اختلال دردناکی است که در اثر رشد بافت اندومتر در محلی غیر از محل اصلی خود (حفره داخلی رحمی) مانند بافتهای تخمدان, روده و یا
بافت لگن ایجاد می شود.
ترشحات دهانه رحم
ترشحات دهانه رحم باعث آسیب رسیدن به اسپرم می شود.
علل ناباروری در آقایان

همانطور که گفته شد مشکلات ناباروری فقط مختص خانمها نیست و ممکن است آقایان اختلالاتی داشته باشند که موجب اخلال در باروری شود.
از علائم ناباروری در آقایان می توان به موارد ذیل اشاره کرد:
- کاهش میل جنسی
- مشکلات نعوذ
- مشکلات انزال
- اختلال در رشد موها
- کوچکی و سفت بودن بیضه ها
- وجود برآمدگی و احساس درد در بیضه ها
- انسداد مجاری اسپرم
- تولید اسپرم کمتر از حد طبیعی
آمادگی لازم قبل از مراجعه به پزشک
- قبل از مراجعه به پزشک جهت بررسی و تشخیص مشکلات باروری لازم است این اقدامات را انجام دهید و با اطلاعات کافی به پزشک مراجعه نمایید.
- لیستی از تمامی داروهایی که خودتان یا همسرتان مصرف می کنید تهیه کنید.
- همه داروهای تجویز شده توسط پزشک و حتی داروهایی که خودسرانه بدون نسخه پزشک مصرف داشته اید همچنین ویتامین ها,مکمل ها و… در این لیست قرار دهید.
- .تعداد دفعاتی که در طول یک هفته و یک ماه رابطه جنسی داشته اید و همچنین تاریخ آخرین رابطه جنسی خود را به خاطر داشته باشید.
- در صورت مشاهده هرگونه تغییرات فیزیکی در بدن حتما آن را به پزشک اطلاع دهید.
- در صورت استعمال دخانیات و یا مصرف الکل حتما میزان و دفعات آن را پزشک اطلاع دهید.
- در صورتیکه سابقه بیماری آمیزشی دارید حتما پزشک را در جریان قرار دهید.
- در صورت ابتلای خود و یا اعضای خانواده به هر بیماری مزمنی مانند دیابت,تیروئید و اختلالات ژنتیکی,حتما پزشک معالج خود را در جریان قرار دهید.
10 روش موثر در درمان ناباروری
پس از طی مراحل اقدامات تشخیصی,نتایج آزمایشها و بررسی های انجام شده و تشخیص نهایی علل ناباروری,پزشکان متخصص زنان و زایمان,آندرولوژیست و همچنین جنین شناس در یک جلسه نتایج بدست آمده از بررسی های انجام شده بر روی زوج را مورد بررسی و تجزیه و تحلیل قرار میدهند و موثرترین روش های درمانی را به زوجین پیشنهاد می دهند و تمام مزایا و معایب روشها را به طور کامل برای زوجین توضیح می دهند و در نهایت این زوجین هستند که تصمیم نهایی را می گیرند.
لازم به ذکر است هر زوج با توجه به علت ناباروری,درمان مخصوص خود را خواهد داشت.
در ادامه روشهای درمانی مختلف را بطور مفصل توضیح داده ایم.
1 # تحریک تخمک گذاری
تحريک تخمک گذاری یک روش درمان دارويي است که برای خانمهایی بکار میرود که تخمک گذاری منظمی ندارند و یا به تنبلی تخمدان, بیماری پلی کیستیک تخمدان و یا اختلال تخمک گذاری دچار هستند.
این روش جهت افزايش تعداد و کيفيت تخمک برای افزايش شانس باروری و موفقيت درمان روش های کمک بارروری (ART) انجام می شود.
داروهایی که در این روش درمانی استفاده می شود داروهای محرک تخمک گذاری هستند که با استفاده از آنها می توان تعداد و کيفيت تخمک ها را
افزایش داد.
پس از حاصل شدن تخمک های مناسب لازم است که زوجین در زمان های خاص و به صورت یک روز در ميان رابطه جنسی داشته باشند.
حدودا در 15 تا 25% از موارد ناباروری اختلال در عمل تخمک گذاری مشاهده می شود,در مواردی که اختلال در تخمک گذاری تنها دلیل ناباروری باشد درمان نتیجه بسيار رضايت بخشی خواهد داشت.
درمان موفقيت آميز در اين موارد به بررسی دقيق و کشف دلیل عدم تخمک گذاری بستگی دارد.
معمولا در مواردی که از روشهای کمک باروری (ART) استفاده می شود, يکی از اقدامات اولیه تحريک تخمک گذاری جهت رسیدن به تعداد مناسبی
تخمک با کيفيت بالا می باشد.
در خانمهایی که تخمدان عملکرد طبیعی و مناسبی دارد برای تهيه تخمک میتوان از سيکل طبيعی استفاده کرد,اما با توجه به اینکه اين روشهای درمانی مستلزم صرف وقت و هزينه می باشند, ترجيح بر این است که برای افزايش شانس باروری از تحريک تخمدان استفاده شود.
جهت تحريک تخمک گذاری در روش های کمک باروری (مانند IVF, ICSI و… ) باید توجه داشت که در کنار به دست آوردن تعداد مناسب تخمک,برای جلوگیری از خطرات احتمالی تا حد ممکن از تحريک بيش از حد تخمدان اجتناب شود.
قبل از شروع هر درمانی لازم است که فرد به طور دقيق و کامل مورد بررسی قرار بگيرد,به اين منظور پزشک علاوه بر معاينات بالینی آزمايشهای لازم را تجویز میکند تا طبق نتايج آزمايشها, بهترین و مناسبترين رژيم درمانی جهت تحريک تخمک گذاری را ارائه دهد و درمان را شروع نمايد.
داروهای مورد استفاده درروش درمانی تحریک تخمک گذاری
داروهای متعددی جهت تحريک تخمک گذاری وجود دارد که طبق نظر پزشک موارد استفاده آنها متفاوت می باشد.
در حال حاضر رایج ترین دارو در تحریک تخمک گذاری ‘کلوميفن سيترات’ می باشد.
زمانی که سطح استروژن,LH و FSH طبيعي است اما در تخمکگذاری اختلال وجود دارد مانند خانمهای مبتلا به PCOS,مناسب ترین دارو برای تحريک تخمک گذاری کلوميفن سيترات می باشد.
درمان با کلوميفن سيترات به این صورت می باشد که روزانه با يک قرص (50 ميلي گرم),از روز سوم تا هفتم يا پنجم تا نهم سيکل قاعدگی شروع می شود و جهت بررسی وضعيت فوليکول ها در روز دهم از سيکل قاعدگی (در صورتیکه شروع درمان از روز سوم باشد) و يا روز دوازدهم از سيکل قاعدگی (در صورتیکه درمان از روز پنجم صورت گرفته باشد) سونوگرافی انجام ميشود.
اگر فولیکول ها به اندازه مورد نظر پزشک (20-18 ميلي متر) رسیده باشند پزشک می تواند با تجويز آمپول HCG زمان تخمک گذاری را مشخص کند.
بهترين زمان رابطه جنسی برای باروری یک تا دو روز نزدیک تخمک گذاری است.این درمان معمولا 3 تا 5 دوره تکرار می شود.
ميزان دوز داروی کلوميفن را تا سه قرص در روز (150 ميلي گرم) میتوان افزايش داد اما بيشتر از آن توصيه نمی شود. احتمال بارداری پس از سه دوره درمان با داروی کلوميفن سيترات 85% و پس از پنج دوره 99% می باشد.
در مواردی که از روش IUI برای باروری استفاده می شود,استفاده از داروی کلومفين سيترات شانس باروری را بالا می برد.
به همین دلیل معمولا پزشک از روز سوم يا پنجم از سيکل قاعدگی به مدت چهار روز برای بيمار روزانه يک تا دو قرص کلومفين سيترات تجويز می کند و پس از آن با انجام سونوگرافی در روز 10 يا 12 از سيکل قاعدگی در صورتیکه اندازه فوليکول ها به 20-18 ميلی متر رسيده باشد با تزريق 5،000 يا 10،000 واحد HCG, بيمار را برای انجام IUI به مدت 38-36 ساعت پس از آن آماده می نمايد.
از دیگر داروهای محرک تخمک گذاری می توان به Human Menopausal Gonadotropin اشاره کرد.
جالب است بدانید داروی HMG به طور طبيعی از ادرار خانمهای يائسه تهيه می شود و حاوی FSH و LH می باشد.
استفاده از داروی HMG با به دقت کنترل شود و جهت پیشگیری از تحریک بیش از حد تخمدان بررسی نتیجه تخمدان بايد به فاصله 2 تا 4 روز يکبار انجام شود.
هدف از درمان با داروی HMG افزايش سطح FSH تا بالای حد لازم برای تحريک رشد تخمدان می باشد و زمانيکه قطر 2 تا 4 عدد از فوليکولهای نهايی بیشتر از 12 ميلی متر برسد دارو با دوز پایین تر تجویز می شود.
در سيکل درمانی IUI, داروی HMG تحت نظر پزشک متخصص به منظور تحريک تخمک گذاری یا به تنهایی استفاده می شود و يا همراه با داروی کلوميفن سيترات مورد استفاده قرار ميگيرد و در سيکل های درمانی لقاح خارج از رحم به همراه ساير داروهای محرک تخمدان تجويز می شود.
یکی دیگر از داروهایی که برای تحريک تخمدان و بدست آوردن تعداد بیشتر فوليکول در سيکل درمانی ART استفاده می شود آگونيست های GnRHa, هورمون رها کننده گنادوتروپين ها می باشد.
آگونيست های GnRHa (سوپرفکت, ديفرلين, دکاپپتيل), هورمون های تزريقی هستند که برای تحريك تخمك گذاری بکار می روند و برای سایر هورمون های بدن كاملا شناخته شده می باشند.
مصرف اين داروها,سطح خونی هورمون محرک فوليكول را افزایش می دهد,اين موضوع به تحريک و رشد تخمک های مضاعف,لانه گزينی و در نهايت بارداری منجر می شود.
استفاده از گونادو تروپين ها علاوه بر اینکه تعداد تخمک ها را افزایش می دهد زمان تخمک گذاری را نیز كنترل میکند و شانس بارداری افزايش می یابد.
در درمانهای کمک باروری هدف از مصرف آگونيست های GnRH کنترل و تنظيم زمان سيکل بيماران می باشد.برای تحریک تخمک گذاری در سيکل IVF و ICSI از درمان همزمان آگونيست های GnRH و گنادوتروپين ها استفاده می شود.
2 # تلقیح داخل رحمی اسپرم (IUI)
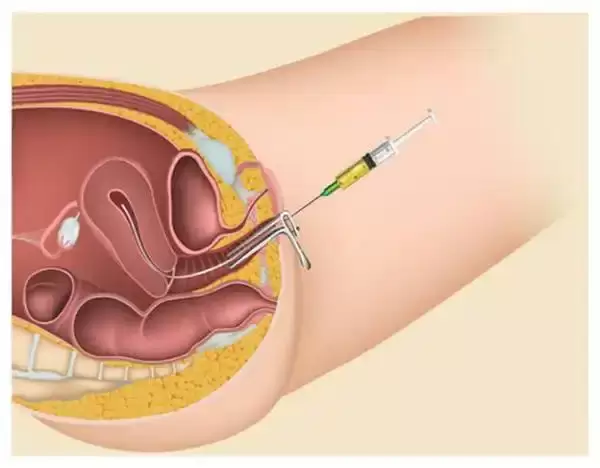
روش IUI عملی نسبتا ساده,کم تهاجم,بدون درد و به نسبت کم هزینه است. در این روش اسپرم مرد به کمک ابزارهای خاصی درون رحم زن قرار داده می شود.
در این روش عمل دریافت تخمک از خانم انجام نمی شود و تخمک گذاری و باروری آن مشابه با روش طبیعی انجام می شود که لازمه آن اطمینان از سلامت لوله های خانم می باشد,بنابراین تلقیح اسپرم به داخل رحم به عنوان یکی از روشهای کمک باروری (ART) محسوب نمی شود.
درواقع تلقیح داخل رحمی یک روش برای درمان ناباروری است و اغلب زوجهای جوان که حداقل یکسال برای بچه دار شدن تلاش کرده اند و نتیجه نگرفته اند این روش را برای درمان انتخاب می کنند.
هدف از انجام IUI,افزایش تعداد اسپرم هایی است که به لوله های رحمی (لوله فالوپ) یعنی محل باروری تخمک می رسند و به این صورت احتمال باروری افزایش می یابد.
در روش درمانی IUI جهت تعیین اندازه فولیکول های در حال رشد حاوی تخمک,از دستگاه سونوگرافی استفاده می شود.
پس از اینکه فولیکولها بطور کامل رشد کردند و تخمکها به مراحل بلوغی مناسبی رسیدند,از هورمون HCG برای تحریک آزاد شدن تخمکها از فولیکول استفاده می شود.
همچنین برای جدا کردن اسپرم های نرمال و متحرک,نمونه مایع منی در آزمایشگاه شستشو داده می شود.
پس از آماده سازی اسپرمهای با کیفیت در آزمایشگاه، مایع منی توسط یک لوله ظریف قابل ارتجاع (کاتتر) از طریق واژن به درون رحم مستقیما تزریق می شود.
این فرآیند باعث می شود تا تعداد سلولهای اسپرم که در رحم قرار می گیرند به بالاترین مقدار برسد و به این ترتیب احتمال بارداری افزایش می یابد. در یک آمیزش جنسی طبیعی تقریبا 10% از کل اسپرم های وارد شده به واژن, به گردن رحم می رسند و با انجام عمل IUI تعداد بیشتری از اسپرم های با کیفیت به داخل رحم راه می یابند.
با توجه به تحقیقات انجام شده,تجویز داروهای محرک تخمک گذاری می تواند شانس باروری را به میزان قابل توجهی افزایش دهد.
بعد از شروع مصرف دارو, سونوگرافي طی روزهای مختلف انجام می شود و زمانی که فولیکول (کیسه حاوی تخمک در تخمدان) به اندازه مناسبی رسید,داروی HCG به صورت عضلانی تزریق می شود,تزریق این دارو موجب بلوغ تخمک و انجام فرایند تخمک گذاری می شود.
40 ساعت بعد از تزریق HCG,بیمار باید مراجعه می کند تا عمل IUI انجام شود. روش IUI زمان بر نیست و مشکل خاصی برای زوج ایجاد نمی کند, این روش معمولا دردناک نیست اما در خانمهایی که نسبت به درد و معاینات زنانه حساس هستند ممکن است عبور کاتتر از گردنه رحم کمی دردناک باشد و گرفتگی ایجاد کند.
این درد و گرفتگی موقتی است و پس از اتمام عمل از بین می رود. اگر هنگام عبور کاتتر گردنه رحم دچار خراشیدگی شده باشد احتمال دارد بعد از عمل لکه بینی جزیی دیده شود که بعد از مدت کوتاهی برطرف می شود.
پس از انجام IUI نیازی به بستری شدن نیست و بیمار کمی بعد از انجام عمل میتواند مرخص شود و فعالیت روزانه خود را آغاز نماید.
توجه داشته باشید این عمل به استراحت مطلق نیاز ندارد اما توصیه می شود پس از ترخیص تا مدتی از انجام فعالیت های سنگین پرهیز نمایید.
روش IUI بسیار ساده است و به روند طبیعی بارداری نزدیک است به همین دلیل بنا به صلاحدید پزشک تا چند نوبت (معمولا 3 تا 4 بار) قابل تکرار می باشد.
در صورتیکه روش IUI موفقیت آمیز نبود بیمار مجددا توسط پزشک مشاوره می شود تا برای انجام روش میکرواینجکشن یا روش IVF تصمیم گیری شود و بهترین راهکار انتخاب شود.
کاربرد روش IUI
معمولا روش تلقیح درون رحمی یا IUI برای زوج هایی پیشنهاد می شود که دارای یکی از شرایط زیر باشند:
1. خانم بارور باشد و آقا مشکلاتی از قبیل :
- کم حجم بودن مایع منی
- کم بودن تعداد اسپرم (کمتر از 5 میلیون اسپرم متحرک نرمال در کل نمونه منی)
- کم تحرکی اسپرم
- اسپرم با شکل غیر طبیعی
- وجود آنتی اسپرم آنتی بادی (Anti sperm Antibodies) در مايع منی داشته باشد, انجام روش IUI میتواند شانس برخورد اسپرم با تخمک را افزایش دهد.
2. در مواردی که مرد به دلیل:
- ناتوانی جنسی
- مشکل در ایجاد نعوظ و حفظ حالت نعوظ
- اختلال در ساختمان آلت تناسلی
- فلج بودن اندام تحتانی
- انزال پس رونده (یعنی شخص به ارگاسم برسد اما انزال نشود و مایع منی از او خارج نشود)
- کاهش میل جنسی
قادر به انزال درون واژن نباشد,استفاده از IUI یک فرصت برای اسپرم است به شرطی که خود اسپرم توانایی لازم برای رسیدن به تخمک و باروری آن را داشته باشد.
3. خانم مشکلاتی در آناتومی یا ترشحات گردن رحم (موکوس سرويکس) داشته باشد، بطور مثال:
- مخاط گردن رحم غلیظ و چسبناک باشد
- در دهانه رحم ترشحات کشنده اسپرم وجود داشته باشد
- مخاط دهانه رحم به قدری کم باشد که اجازه عبور به اسپرم داده نشود
روش IUI این امکان را برای اسپرم فراهم می کند که بتواند بدون نیاز به عبور از مخاط گردن رحم مستقیما به داخل رحم تزریق شود.
4. درصورتیکه ناباروری ناشی از اختلالات ایمنی باشد
- یا خانوم به دلیل درد هنگام رابطه جنسی یا شرایطی مانند ابتلا به واژينيسم (واژینیسموس یا انقباض غيرارادی عضلات واژن بطوریکه تماس جنسی را غير ممکن می کند) امکان مقاربت طبیعی را نداشته باشد.
5. خانم به اندومتريوز مبتلا باشد:
- خانم هایی که به درجات مختلف از اندومتريوز مبتلا می باشند و یا در تخمک گذاری مشکل دارند.
روش IUI در زوجهایی که مدت باروری طولانی شده و به اصطلاح دچار ‘ناباروری نامشخص’ شده اند می تواند موثر باشد. روش IUI در خانمهای کمتر از 35 سال معمولا موفقیت بالاتری نسبت به خانمهای بالای 35 سال دارد.
در روش IUI مانند سایر روشهای تلقیح خارج رحمی,میزان موفقیت ابتدا به سلامت و کیفیت اسپرم و تخمک بستگی دارد.
3 # لقاح مصنوعی (IVF)
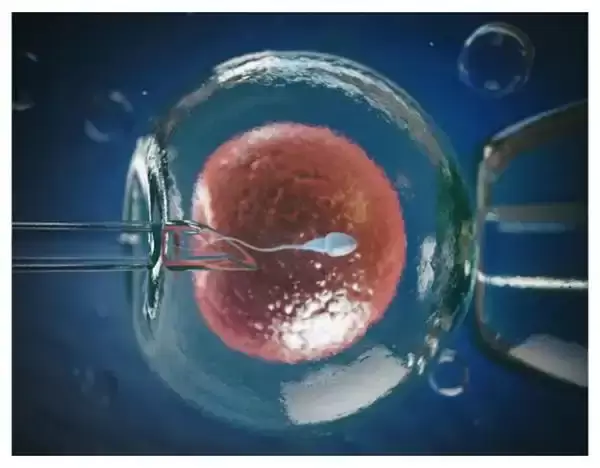
یکی از با سابقه ترین روشهای کمک باروری (ART) روش IVF می باشد. این روش به این صورت است که پس از تحریک تخمدان ها و تخمک گذاری,تخمکها و اسپرم استخراج می شوند و لقاح در خارج از رحم انجام شده و بعد از تشکیل جنین در محیط آزمایشگاه, جنین را به داخل رحم منقل می کنند.
روش IVF معمولا در مواردی بکار می رود که شرایط رسیدن اسپرم به تخمک در رحم فراهم نباشد.
در شرایطی از درمان IVF استفاده می شود:
- انسداد لوله های رحمی
- چسبندگی لگنی
- تعداد کم و تحرک پایین اسپرم
از روش IVF برای لقاح استفاده می شود. علاوه بر این در مواردی که سایر روشهای کمک درمانی ساده مانند تحریک تخمک گذاری و یا عمل IUI ناموفق باشد,عملIVF گزینه مناسبی برای زوجین می باشد.
سیکل IVF به این صورت است که تخمکهای بالغ از تخمدانها برداشته می شود و در محیط آزمایشگاهی در مجاورت با اسپرم قرار داده می شود تا تخمک بارور شده و عمل لقاح انجام شود. تخمک بارور شده در شرایط مناسبی کشت داده می شود و پس از رخ دادن تقسیمات جنینی در رحم مادر قرار داده میشود.
با توجه به مراحل تکامل جنین و شرایط رحم,جنین بین روزهای 3-2 یا 6-5 پس از تخمک گیری به رحم مادر منتقل می شود.
مراحل انجام IVF به چه صورتی است ؟
به طور کلی درمان IVF در هفت مرحله یه شرح ذیل انجام می شود:
مرحله اول
تـحریک تخمدان و بررسی رشد فـولیکول ها
مرحله دوم
جمع آوری تخمکها (عمل پانکچر یا تخمک گیری)
مرحله سوم
تهيه و آماده سازی اسپرم
مرحله چهارم
لقاح و رشد جنين در محيط آزمايشگاهی
مرحله پنجم
انتقال جنين به داخل رحم مادر
مرحله ششم
مصرف دارو در حین انتقال و پس از انتقال جنين
مرحله هفتم
بررسی وضعیت بارداری و انجام تست بارداری
موارد كاربرد IVF
روش IVF در تمام مواردی كه رحم شرايط رسيدن اسپرم به تخمک را نداشته باشد بکار می رود.
1. شرایطی که مانع از رسیدن اسپرم به تخمک می شود عبارتند از:
- انسداد لوله های رحمی
- چسبندگی حفره لگنی
- تعداد كم اسپرم
- تحرک پايين اسپرم
2.مشکلات لوله های رحمی
زمانی که خانمها با مشکلاتی مثل بسته بودن لوله فالوپ,چسبندگی لوله ها یا حفره های لگنی مواجه باشند یا اگر طی حاملگی خارج رحمی لوله های آن ها برداشته شده باشد و يا خودشان اقدام به بستن لوله های رحمی کرده باشند روش درمانی IVF به عنوان یک راهکار درمانی موثر پیشنهاد می شود.
3.آندومتريوز
احتمال بارداری با روش IVF در خانمهایی که مبتلا به آندومتریوز می باشند و درمانهای دارویی و جراحی موفقیت آمیز نبوده است بسیار بالا می باشد.
4.مشکلات مردانه
آقایانی که با مشکلاتی نظیر کاهش در تعداد يا اخلال در حرکت اسپرم و يا وجود آنتی بادی ضد اسپرم مواجه هستند روش IVF میتواند موثر باشد.
5.نازایی با عللی ناشناخته
حدودا در 10% از موارد نازایی برخلاف تمام ارزيابی های انجام شده,علت مشخصی برای نازایی بدست نمی آید,در این موارد که با عنوان ‘ناباروری با علت نامشخص’ تعریف می شود پس از انجام چند مرحله IUI ناموفق,روش IVF انتخاب می شود.
6.نازايي به علت مشکلات ايمنولوژيک
سیستم ایمنی بعضی از خانمها عليه اسپرم مرد ماده ای بنام آنتی بادی ضد اسپرم ترشح می کند كه باعث از بین رفتن اسپرم ها می شود و يا آنها را غيرفعال می كند.
این حالت نازایی ايمنولوژيک بشمار می رود و پس از انجام چند مرحله IUI ناموفق در نهایت روش IVF انتخاب می شود.
4 # میکرواینجکشن یا تزریق اسپرم داخل تخمک (ICSI)
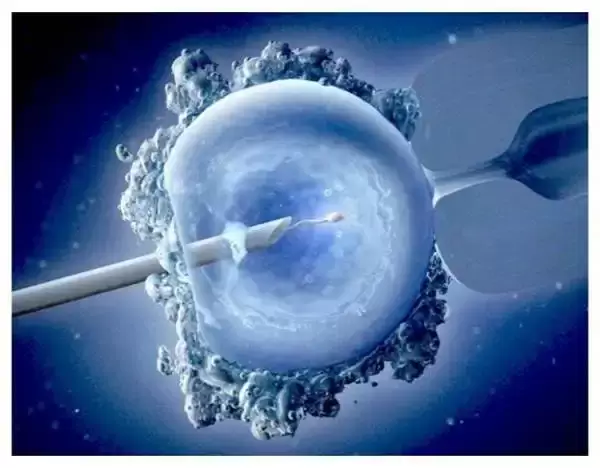
میکرواینجکشن یکی از تکنیکهای کمک باروری (ART) است که به کمک روشهاى پيشرفته,یک اسپرم را مستقیما به داخل تخمک تزریق می کنند و برای مدت مشخصی در دستگاه انکوباتور (دستگاهی جهت کشت و رشد دادن نمونه های زنده) کشت می دهند تا لقاح,تقسیم سلولی و تشکیل جنین صورت گیرد.
تزریق اسپرم درون سیتوپلاسم نشان می دهد که تا زمانی که اسپرم وجود داشته باشد حتی به تعداد بسیار کم,باروری امکان پذیر است.
درواقع میتوان گفت روش میکرواینجکشن در مواردی استفاده می شود كه اسپرم از لحاظ تعداد,تحرک و ظاهر,كيفيت مطلوب را نداشته باشد و یا چندين مرحله عمل IVF ناموفق انجام شده باشد.
توجه داشته باشید روش میکرواینجکشن تضمینی برای بارداری قطعی نیست,اما می تواند فرآیند پیچیده باروری را آسان تر کند.
مراحل انجام میکرواینجکشن
مراحل انجام میکرواینجکشن کاملا مشابه با مراحل IVF است, با این تفاوت که بجای بارور شدن تخمک در ظروف آزمایشگاهی,یک متخصص جنین شناس اسپرم های با کیفیت مطلوب,از نظر تحرک و ظاهر نرمال را از نمونه مایع منی استخراج می کند و بطور مستقیم در هر تخمک یک اسپرم تزریق می کند.
در واقع مراحل تحریک تخمدان,جمع آوری تخمک و تهیه اسپرم صورت می گیرد اما در مرحله چهارم برخلاف روش IVF که اسپرم و تخمک در ظرفی کنار هم قرار داده می شود تا اسپرم خودش وارد تخمک شود و آن را بارور کند,در روش میکرواینجکشن,اسپرم به داخل تخمک تزريق می شود و به دنبال آن لقاح صورت می گیرد.
در روش میکرواینجکشن متخصص جنين شناس با استفاده از یک ميكروسكوپ با بزرگنمايی بالا می تواند اسپرم های طبيعی را از اسپرم های غير طبيعی تشخیص دهد و پس از بی حركت كردن اسپرم با استفاده از یک سوزن بسيار نازک آن را به داخل تخمک تزريق می کند و در پی آن تقسیم سلولی و تشکیل جنین صورت می گیرد.
بارور کردن تخمک با روش میکرواینجکشن نیازی به استفاده از تعداد زيادی اسپرم ندارد و برای هر تخمک فقط يك اسپرم تزريق می شود.
پس از اینکه جنین تشکیل شد,انتقال آن به داخل رحم و باقی مراحل مانند روش IVF انجام می شود.
انجام میکرواینجکشن در یک سیکلIVF, احتمال بارداری را افزایش می دهد اما پس از بارداری هیچ تاثیری در موفق بودن بارداری ندارد.
برخی پزشکان بر این باورند که بهتر است که انتقال جنین در مرحله بلاستوسیست انجام شود. یعنی تخمکهای بارور شده حدودا 5-6 روز در محیط خارج رحم بمانند تا تکامل خود تا مرحله بلاستوسیست را طی کنند و سپس به رحم منتقل شوند. در انجام عمل ميكرواينجكشن مانند روش IVF به منظور افزايش درصد موفقيت چندين تخمک لقاح می يابد بنابراین تعداد جنين های تشكيل شده زياد است, اما تعداد جنین هایی که قابل انتقال به مادر می باشند به سن مادر, کیفیت جنین ها, تعداد دفعاتی که قبلا روشهای درمانی باروری انجام شده و همچنین به وضعیت رحم مادر نیز بستگی دارد.
درصورتیکه سایر جنين ها مناسب باشد و كيفيت مطلوبی داشته باشند, با رضایت زوجین تعدادی از آنها فریز شده و نگهداری می شوند تا در صورت نياز برای بارداری های بعدی استفاده شود.
کاربرد روش میکرواینجکشن
- تعداد اسپرم های پدر بسیار کم باشد.
- اسپرم دچار مشکلاتی مانند کم تحرکی و ظاهر غیر طبیعی باشد.
- تلاش های گذشته جهت انجام لقاح خارج رحمی موفقیت آمیز نبوده باشد.
- آقایانی که سابقه وازکتومی دارند و باید اسپرم را از بیضه ها یا اپیدیدیم (محل بلوغ اسپرم) برداشت کرد.
- در شرایطی که تعداد اسپرم در مایع منی صفر است اما در بافت بیضه اسپرم وجود دارد. (آزواسپرمی غیر انسدادی)
- آقایانی که در انزال مشکل دارند مانند افرادی که دچار آسیب نخاعی, دیابت و یا اختلالات دیگری هستند.
5 # بلوغ تخمک در آزمایشگاه (IVM)
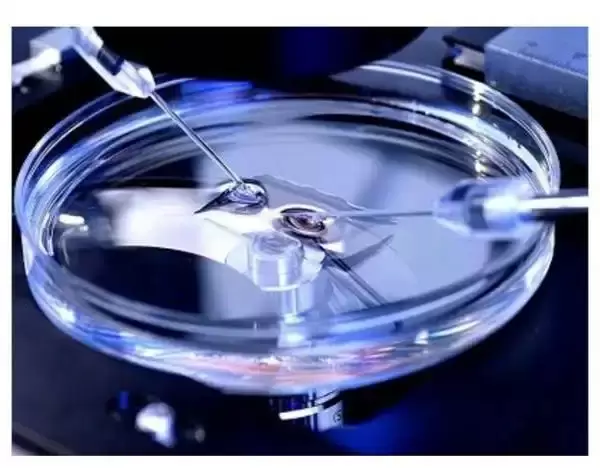
تخمدان های پلی کیستیک یکی از مواردی است كه در بررسی علل نازایی به عنوان یکی از اصلی ترین دلایل نازایی شناخته شده است. شایع ترین علت عدم تخمک گذاری سـندرم تخمدان پلی كيـستيک (PCOS) می باشد كه تا الان علت خاصی برای آن شناسايی نشده است. درصد قابل توجهی از افرادی که مشکل ناباروری دارند خانمهایی هستند که به سندرم تخمدان پلی کیستیک مبتلا می باشند.
بزرگترین مشکل اين افراد عدم تخمک گذاری می باشد. متداول ترین روش برای درمـان خانمهای مبتلا به تخمدان پلی کیستیک, تحريـک تخمـک گـــذاری با داروی کلـوميفن ســـيترات و گونــادوتروپين ها می باشد.
لازم به ذکر است استفاده از این داروها باعق تحريک پذيری شديد تخمـدانهـا می شود و ممکن است برای افراد خطر آفرین باشد.
از جمله خطراتی که ممکن است برای افراد ایجاد شود میتوان به خطـر بـروز سـندرم تحریک بـيش از حـد تخمـدان (OHSS) و آسيت (تجمع مايع در حفره شكمی) اشاره کرد.
بلوغ تخمک در شرایط آزمایشگاهی یا IVM یکی از روش های درمانی جديد که برای حل اين مشكل ارائه شده است. در روش IVM بـه جـای تلاش برای رشد فوليكول ها در بدن تا اندازه 20-18 ميلي متر (مرحله متافـاز II) به کمک یک سوزن مخصوص و استفاده از سونوگرافی واژينال,تخمک های نابالغ با قطر 2 تا 10 میلی متر استخراج می شود سـپس تخمـک هـای نابالغ,در شرايط آزمايشگاه تـا رسیدن به مرحلـه بلـوغ كـشت و نگهـداری می شوند.
در واقع می توان گفت روش IVM به نوعی مانند روش IVF می باشد,یعنی تخمک ها جمع آوری می شوند و در محیط آزمایشگاه با اسپرم لقاح داده می شوند (لقاح معمولا با استفاده از روش میکرواینجکشن صورت میگیرد, نتایج بدست آمده نشان می دهد که میزان لقاح با استفاده از روش ICSI نسبت به IVF در این روش بیشتر است) سپس کشت داده می شوند تا جنین تشکیل شود و عمل انتقال جنین به رحم صورت گیرد.
تفاوت روش IVF و IVM در این است که عمل تخمک گیری در روش IVM زمانی انجام می شود که تخمک ها هنوز نابالغ هستند,به این معنی که در روش IVM برخلاف روش IVF نیازی به تخمکهای بالغ نیست و لازم نیست مانند روش IVF,خانمها پیش از جمع آوری تخمک ها دارو مصرف کنند تا تخمک ها بالغ شوند.
پس از عمل پانکچر (تخمک کشی) و استخراج تخمک های نابالغ,روند بلوغ تخمکها به جای بدن در شرايط آزمايشگاهی و محيط كشت شامل تركيبات مورد نياز برای بلوغ تخمک (حاوی مواد مغذی و هورمونهای مورد نیاز) و قرارگیری در انکوباتور به مدت 24 تا 48 ساعت,انجام می شود پس از این باقی مراحل مانند IVF به ترتیب صورت می گیرد.
گاهی مواردی مشاهده می شود که حتی پس از تحریک تخمک گذاری توسط دارو و انجام عمل تخمک کشی,همه یا تعدادی از تخمک هایی که از پانکچر به دست می آید نابالغ باشند,در این شرایط می توان از روش IVF بهره گرفت و آنها را در شرایط آزمایشگاهی کشت داد تا به بلوغ نهایی برسند.
6 # انتقال جنین در مرحله بلاستوسیست
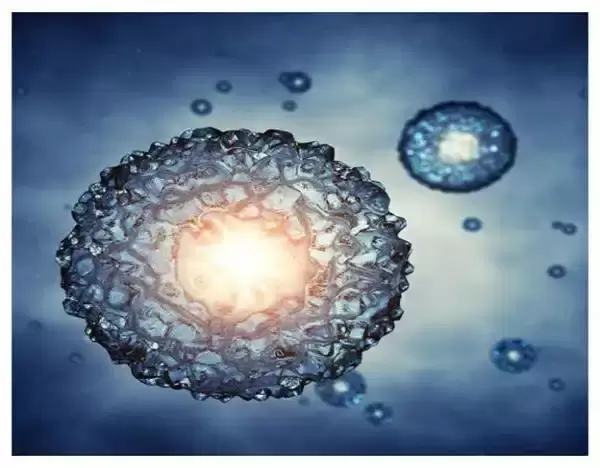
معمولا انتقال جنين در روشهای کمک باروری لقاح خارج از رحم (ART) دو روز پس از تخمک گیری (اووسيت) یعنی در مرحله امبریو یا زمانی که جنين در مرحله 2 يا 4 سلولی می باشد,صورت می پذیرد. در واقع میتوان گفت این زمانی است که تخمک پس از لقاح به طور طبيعی به رحم می رسد و رحم شرایط مناسبی برای بقای جنین دارد.
در برخی شرایط با توجه به تعداد تخمک های لقاح یافته و سابقه بیمار و همچنین صلاحدید متخصص جنین شناسی,جهت انتخاب جنین بهتر با رشد و کیفیتی مناسب و نیز بهبود کیفیت لانه گزینی جنین می توان کشت جنینها و انتقال آنها را تا روز سوم یا درواقع مرحله بلاستوسیست ادامه داد به این دلیل که انجام بارداری موفقیت آمیز مستلزم اتصال بلاستوسیت به دیواره رحم می باشد.
بلاستوسیت در حقیقت جنین یا رویانی است که بعد از لقاح,به مدت 5 تا 6 روز رشد کرده و به دو نوع سلول مختلف تقسيم شده است.
این دونوع سلول مختلف شامل تروفکتودرم یا سلولهای سطحی که جفت را تشكيل می دهند و توده سلولی داخلی,که تبديل به جنين می شود می باشد.
يك بلاستوسيست سالم در روز ششم از مخاط پوششی خود خارج می شود و 24 ساعت پس از خارج شدن در مخاط داخلی رحم قرار می گيرد.
جهت رسیدن به مرحله بلاستوسیت ابتدا جنین درون انکوباتور در بخش جنین شناسی کشت داده می شود تا تکامل بيشتری پيدا کند,در طی این مرحله معمولا جنین هایی که دچار اختلالات ژنتیکی هستند یا کروموزوم غیر طبیعی دارند از بین می روند,بنابراین پس از گذشت این زمان و رشد مناسب جنين,می توان یک یا دو جنین که کيفيت مناسب و پتانسيل رشد بـیشتری دارند,جهت انتقال به درون رحم مادر انتخاب کرد و عمل انتقال را انجام داد که همین امر می تواند در موفقيت روشهای کمک باروری بسیار موثر باشد.
فعال شدن ژنوم جنينی (محتوای ژنتیکی هر فرد شامل DNA هسته, کلروپلاست و میتوکندری می باشد)پس از مرحله 4 يا 8 سلولی رخ می دهد, درنتیجه تعيين کيفيت جنين طبق ژنوم جنينی در روز دوم امکان پذير نمی باشد و نمی توان بطور دقیق جنین را انتخاب کرد.
لازم به ذکر است انتقال جنين با کيفيت مناسب موفقيت روشهای کمک باروری را به ميزان 40 تا 50 درصد افزایش می دهد.
تعداد جنین هایی که در مرحله بلاستوسیست انتقال داده می شوند کمتر از تعداد جنین هایی است که در مرحله امبریو (در دو روز اول) منتقل می شوند,زیرا قدرت اتصال بلاستوسیست به جداره رحم در مقایسه با مراحل تکامل قبلی جنین بسیار بیشتر است.
در حال حاضر در اکثر کشورهای دنیا در هر سیکل درمانی فقط یک بلاستوسیست منتقل میشود که این موضوع یکی از مزایای انتقال جنین در مرحله بلاستوسيست به شمار می رود,زیرا یکی از اهداف اصلی لقاح آزمایشگاهی,ايجاد حاملگی تك قلویی داخل رحمی است و در این روش می توان جنین های كمتر اما با کیفیت بالا و مطلوب تری را منتقل کرد که باعث کاهش احتمال حاملگی چند قلويی و عوارض ناشی از آن و همچنین افزایش آمار زايمان های سالم می شود.
برخلاف فوايد انتقال جنين در مرحله بلاستوسيست مانند افزایش احتمال لانه گزینی, كـاهش احتمال چندقلويـی و امكـان ارزيابی ژنتيكی جنين,انتقال بلاستوسيست برای همه زوجها مناسب نيست و با اندکی ریسک همراه است.
در تعداد اندکی از بيماران هيچ یک از جنین ها به مرحله بلاستوسيست نمی رسند و به تدريج از بين می روند که اين موضوع منجر به از بين رفتن كل جنین ها می شود.
تصميم گيری برای كشت و انتقال بلاستوسيست به عوامل زیر بستگی دارد:
- سن بيمار
- سن تخمک
- تعداد تخمک های بارورشده
- موفقيت قبلی لقاح خارج از رحم
- كيفيت جنین (رويان)
- شمارش سلول در روز سوم انجام كشت
طبق تحقیقات بدست آمده كشت و انتقال تا مرحله بلاستوسيست برای این افراد نتایج بهتری خواهد داشت:
- بيماران جوان تر
- بيمارانی كه از اهداكنندگان جوان تر تخمک دريافت می کنند
- بيمارانی که تخمک بيشتری توليد می كنند
- بيمارانی كه سابقه لقاح خارج از رحمی موفقيت آميز داشته اند.
فرآیند انتقال بلاستوسیت
بطور کلی انتقال بلاستوسیت شبیه به انتقال جنین در مرحله مورولا به رحم است با این تفاوت که اتصال جنین به جداره رحم پس از گذشت 2 تا 3 روز انجام می شود به این دلیل که بلاستوسیت 5 الی 6 روز قبل از انتقال, مراحل تکاملی خود را در بخش جنین شناسی درون انکوباتور طی کرده است.
7 # تلقيح نطفه داخل لوله رحم (GIFT)
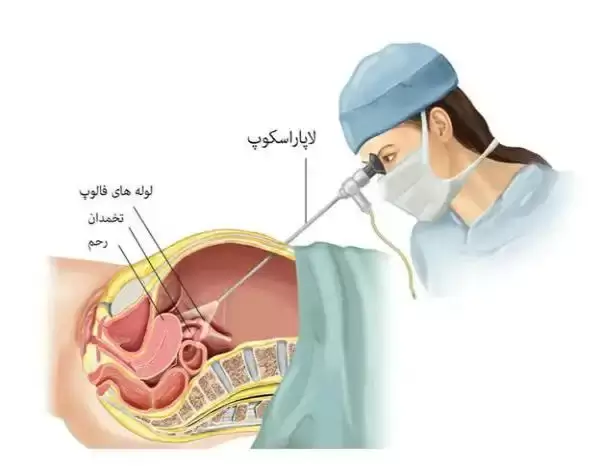
روشGIFT معمولا در موارد استفاده از رحم جایگزین به کار می رود. این روش تا مرحله جمع آوری کردن تخمک و تهيه و آماده سازی اسپرم مشابه با روش IVF است اما بعد از اين مرحله مقدار مناسبی از اسپرم و تخمک توسط لاپاراسكوپ (یک لوله بلند و نازک که دارای یک دروبین با وضوح بالا و یک لامپ می باشد) مستقیما در داخل لوله های رحمی قرار داده می شود و شرط انجام آن داشتن لوله رحمی سالم می باشد.
همانطور که می دانید لوله های رحمی در حالت طبیعی محل لقاح می باشند.
معمولا روش ZIFT و GIFT از راه لاپاروسکوپی انجام می شود,گاهی برخی از پزشکان به جهت کاهش هزینه برای بیمار این دو روش را بصورت واژینال انجام می دهند اما با این حال با توجه به پیشرفت روشهای درمانی دیگر استفاده از دو روش ZIFT و GIFT در رحم جایگزین به علت مخارج بالایی که برای بیماران دارد کمتر توصیه می شود.
اين روش نسبت به تکنیکهای دیگر کمتر متداول است اما گاهی برای زوج هايی که به دلايلی ناشناخته نابارور هستند یا ناباروری آنها ناشی از عواملی چون اختلالات دستگاه ايمنی,مشکلات دهانه رحم و همچنین آندومتريوز مختصر رحم می باشد به کار می رود.
8 # انتقال نطفه بارور شده به داخل لوله رحم (ZIFT)
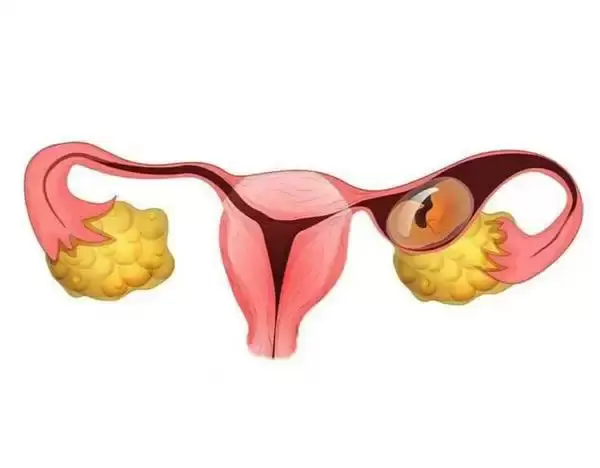
تکنیک ZIFT یا انتقال سلول تخم بارور شده به درون لوله های رحمی يکی از روشهای کمک باروری است که تركيبی از روشهای IVF و GIFT می باشد. در این روش بيماران مشابه با مراحل IVF آماده می شوند,تخمک ها جمع آوری می شود,لقاح در آزمایشگاه صورت می گيرد زیگوت تشکیل می شود, تا این مرحله همه چیز مشابه با روش IVF می باشد اما در مرحله انتقال پس از انتخاب جنین ها (مرحله تک سلولی) با توجه به کيفيت جنين ها و شرايط رحم و سن مادر تعداد مناسبی از آنها با توجه به صلاحدید پزشک به کمک لاپاراسکوپی در لوله های رحم یعنی لوله فالوپ قرار داده می شود.
اين روش در مواردی انجام می شود كه انتقال جنين از دهانه رحم و راه واژینال امکان پذیر نباشد و یا مشكل باشد.
تفاوت روش ZIFT با GIFT
تفاوت این دو روش در این است که در روش ZIFT جنین های لقاح یافته در آزمایشگاه,به لوله های رحمی انتقال داده می شود در حالیکه در روش GIFT مخلوطی از تخمک و اسپرم به این لوله ها منتقل می شود.
معمولا دو ساعت پس از انتقال جنين با لاپاراسکوپی خانم ها می توانند از مراکز درمانی مرخص شوند و توصيه میشود حداقل سه روز در منزل استراحت مطلق داشته باشند و در صورت امکان از توالت فرنگی استفاده نمايند.
سایر مراحل مشابه با روش IVF انجام می شود. یکی دیگر از موارد کاربرد ZIFT پاسخ ضعیف تخمدان خانم می باشد به عبارت دیگر فرد تعداد تعداد کمی تخمک و رویان دارد که همین موضوع یکی از عوامل رایجی است که منجر به درمان ناموفق یک سیکل درمانی IVF یا روش میکرواینجکشن می شود.
در چنین مواردی روش ZIFT یا درواقع همان انتقال مستقیم جنین به داخل لوله فالوپ به کمک لاپاراسکوپی پیشنهاد می شود.
این نکته قابل توجه است که برای این افراد,از تخمک گذاری با استفاده از دوز بالای داروی HMG که باعث ایجاد تخمک های بیشتر می شود استفاده می گردد.
در برخی از موارد ناباروری احتمال موفقیت آمیز بودن روش ZIFT نسبت به IVF و میکرواینجکشن بیشتر است,به این دلیل که رویان (جنین) مستقیما به جایی که به آن تعلق دارند فرستاده میشود یعنی لوله فالوپ.
در روشهایی چون GIFT و ZIFT به این دلیل که میزان باروری تخمک, پیشرفت روند باروری و همچنین کیفیت جنین های تولید شده قابل ارزیابی نیست,اغلب تعداد جنین های بیشتری منتقل می شود و این موضوع می تواند منجر به بارداری های چند قلویی و یا حاملگی خارج از رحم شود. در روش میکرواینجکشن به دلیل اینکه تعداد جنین کمتری به رحم منتقل می شود احتمال حاملگی خارج از رحم و بارداری چند قلویی نیز کاهش می یابد و درصد موفقیت این روش درمانی نیز بیشتر می شود.
در روشهای نوین درمان ناباروری مانند میکرواینجکشن برخلاف روش GIFT و ZIFT تخمک و اسپرم با بالاترین کیفیت انتخاب می شوند و با تزریق اسپرم به داخل تخمک در محیط آزمایشگاهی میتوان از روند تشکیل جنین اطمینان حاصل کرد.
9 # هچینگ آزمایشگاهی جنین
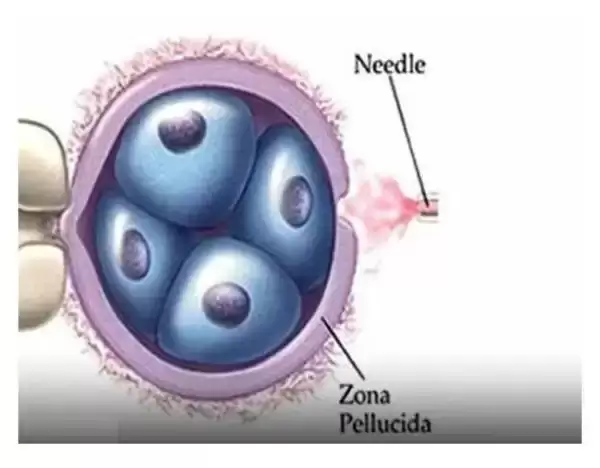
هیچینگ آزمایشگاهی جنین یک اصطلاح است که به باز کردن پوسته محافظ سلولهای جنینی گفته می شود.
تخمک از زمانی که از تخمدان آزاد می شود,پس از باروری و شکل گیری جنین تا مرحله لانه گزینی جنین در جداره رحم یا اندومتر توسط یک پوشش نرم خارجی به نام زوناپلوسیدا محافظت می شود.این پوسته ژلاتینی مانند از مواد قندی و پروتئینی تشکیل شده است و باعث محافظت از تخمک و جنین می شود.
درواقع به این معنی که پس از وارد شدن یک اسپرم به داخل تخمک,زونا پلوسیدا مانع از ورود اسپرم های بعدی می شود و همچنین پس از لقاح موجب هدایت جنین از لوله رحم به سمت رحم می شود که مانع از جداشدن سلول های جنین از یکدیگر می گردد.
جنین قبل از لانه گزینی در اندومتر باید خود را از داخل این پوسته خارج نماید. پس از رسیدن جنین به حفره رحم و تشکیل بلاستوسیست در روز پنجم پس از لقاح,به صورت طبیعی این پوسته نازک می شود و به کمک آنزیم هایی که از جنین و دیواره رحم ترشح می شوند پاره می شود.
این فرآیند پاره شدن هچینگ نامیده می شود که امکان چسبیدن جنین و نفوذ آن به داخل دیواره رحم را فراهم می کند و نتیجه آن بارداری است. به عبارت دیگر هیچینگ به معنی خروج جنین از پوسته خود می باشد.
در صورتیکه مرحله هچینگ با موفقیت انجام نشود بارداری رخ نمی دهد. گاهی دیده می شود که در بعضی از موارد زوناپلوسیدا ضخیم تر از حد نرمال است, این موضوع باعث کاهش احتمال لانه گزینی جنین در اندومتر می شود.
در مواردی که لقاح آزمایشگاهی صورت میگیرد عواملی وجود دارد که مانع از نازک شدن زوناپلوسیدا و پارگی آن در اثر آنزیم ها می شوند. عواملی چون بالا بودن سن مادر,بالا بودن سطح FSH در خون مادر و شرایط ناشی از محیط کشت باعث مقاومت و نفوذ ناپذیری زونا پلوسیدا می شود در نتیجه شانس لانه گزینی و حاملگی کاهش می یابد.
در صورت مواجهه با این موارد با استفاده از لیزر هچینگ,جنین بواسطه ایجاد یک شکاف کوچک در لایه زوناپلوسیدا از آن خارج می شود,این امر باعث تسهیل لانه گزینی یعنی چسبیدن به دیواره رحم و در نهایت افزایش شانس بارداری می شود.
لیزر هچینگ یک تکنیک آزمایشگاهی بجهت بهبود بخشیدن به سایر روشهای کمک باروری مانند IVF و ICSI است.
علاوه بر این برای بیمارانی که دوره انتقال جنین منجمد شده دارند نیز استفاده می شود.
این روش باید قبل از انتقال جنین به رحم و در مراحل ابتدایی تشکیل جنین یعنی روزهای دوم یا سوم بعد از تشکیل زیگوت و یا در مرحله بلاستوسیت یعنی روز پنجم یا ششم پس از تشکیل زیگوت انجام شود.
مزایا و معایب هیچینگ آزمایشگاهی
مزایا
- فراهم کردن چسبندگی سلولهای جنین به دیواره رحم امکان باردار شدن مادرانی که سطح FSH خون بالایی دارند.
- استفاده از روشهای مکانیکی و شیمیایی و همچنین لیزر جهت پاره کردن لایه زوناپلاسیدا.
معایب
- عدم کارایی لازم جهت بارور شدن به این روش
- بارداری نیمه تمام و زایمان زودرس
- احتمال به خطر افتادن و اختلال در سلامت جنین
این روش برای برای خانمهای جوان و جنین های سالم قابل استفاده نمی باشد.
انواع هچینگ آزمایشگاهی
- شیمیایی
- مکانیکی
- لیزر
هیچینگ شیمیایی:
در این روش از مواد شیمیایی به منظور تحلیل رفتن و ضعیف شدن دیواره زوناپلاسیدا استفاده می شود.
انجام هیچینگ شیمیایی بسیار مشکل است و نتیجه آن به مقدار ماده شیمیایی مورد استفاده بستگی دارد.
استفاده مقادیر زیاد از این مواد شیمیایی برای جنین بسیار مضر است.
هیچینگ مکانیکی:
در روش مکانیکی با استفاده از یک ابزار کوچک مانند سوزنی که در ICSI استفاده می شود, حفره کوچکی در زوناپلاسیدا ایجاد می شود.
موفقیت و نتیجه این روش به میزان مهارت متخصص جنین شناسی بستگی دارد تا در حین انجام آسیبی به جنین وارد نشود.
لیزر هیچینگ:
این روش به این صورت است که از یک سیستم میکرو لیزر برای ایجاد یک برش کوچک در زونا پلاسیدا استفاده می شود.
اشعه این لیزر کاملا کنترل شده به بخشی از زوناپلوسیدا تابیده می شود و حدود 35 تا 40 میکرومتر از لایه را حذف می کند.
این فرآیند لیزر هچینگ نامیده می شود. با توجه به اینکه این روش فقط زوناپلوسیدا یعنی لایه خارجی را تحت تاثیر قرار می دهد اثر نامطلوبی بر جنین ها نمیگذارد و نوزادانی که در دوران جنینی آنها از این روش استفاده شده است سالم هستند.
این تکنیک در مقایسه دو تکنیک شیمیایی و مکانیکی درصد موفقیت بالاتری در باروری دارد و به مهارت متخصص جنین شناسی بستگی ندارد.
موارد کاربرد هیچینگ
توجه داشته باشید که هچينگ آزمايشگاهی نبايد روی هر جنينی انجام شود.
طبق تحقیقات به دست آمده زمانیکه هچينگ روی جنينهای سالم انجام بشود, احتمال جايگزينی جنين در داخل دیواره رحم را كاهش می دهد. بنابراين هچينگ فقط بايد در موارد مشخص و واجد شرایط انجام شود. در اين موارد فقط جنينهای مشخص شده از قبل طبق دستورالعمل مربوط انتخاب می شوند. علاوه بر این اين روش محدود به گروهی خاص از بيماران نابارور است.
منظور از گروه خاص بیمارانی است که دارای این ویژگیها باشند:
ویژگیهای مادر:
- خانمهایی با سن 38 سال و يا بالاتر
- خانمهایی که سطح هورمون FSH در آنها بسیار بالا می باشد.
- خانمهایی با سابقه انتقال جنين و عدم بارداری (سابقه دو یا چند بار شکست در روش IVF)
- خانم هایی که برای اولین بار IVF یا ICSI انجام میدهند اما به دلیل نیاز به سطح بالایی از گونادوتروپین ها در اثر مشکلات تخمدان,شانس کمی برای باروری دارند.
ویژگیهای جنين:
- جنین با پوسته ضخیم بطوریکه ضخامت زوناپلوسيدا بيشتر از 17 ميكرومتر باشد.
- جنین با رشد و نمو آهسته و کند و نامناسب بطوریکه رشد جنين در روز سوم كمتر از 5 سلول باشد.
- ميزان فراگمنتيشن در جنين بالاتر از 20% باشد.
10 # تشخیص اختلالات ژنتيکی جنین قبل از لانه گزینی (PGD)
روش PGD یک فناوری جدید در بررسی ژنتیکی و تشخیص اختلالات احتمالی جنین قبل از لانه گزینی در رحم مادر است.این روش برای افرادی که دارای شرایط خاص وراثتی هستند این امکان را بوجود می آورد تا از انتقال ژنهای معیوب به فرزندان جلوگیری نمایند. PGD شامل بررسی همه روشهای آزمایش سلولهای جنین از جمله بررسی کروموزوم ها و ژنهای جنینی قبل از انتقال به رحم مادر در طول یک دوره IVF/ICSI می باشد.
ابتلای زوجین یا خانواده آنها به بيماری ژنتيكی ,بالا بودن سن مادر و سایر عواملی از این قبیل موجب افزايش احتمال بروز ناهنجاریهای كروموزومی در نوزاد می شود.
در گذشته برای جلوگیری از تکرار بیماریهای ژنتیکی روش PND و امروزه روش PGD بکار می رود.
تفاوت روش PND و PGD
روش PND اختلالات ژنتیکی را در حین بارداری ناشی از لقاح طبیعی تشخیص می دهد. تشخیص ژنتیکی معمولا بین هفته 10 تا 14 بارداری صورت می گیرد و در صورتیکه اختلال در کروموزوم ها تشخیص داده شود تنها توصیه ختم بارداری می باشد.
در روش PGD چون لقاح غیر طبیعی و به صورت خارج رحمی (IVF/ICSI) انجام می شود فقط جنین هایی به رحم مادر منتقل می شوند که در بررسی های ژنتیکی سالم بوده اند در نتیجه هیچ گونه صدمات جسمی و عاطفی و یا سقط جنین را به دنبال نخواهد داشت.
در واقع می توان گفت روش PGD تنها روش موثر برای زوجهایی است که در معرض به دنیا آوردن فرزندی مبتلا به بيماريهای ژنتيکی قرار دارند اما به دلایل قانونی یا اعتقادی و مذهب حاضر به سقط جنين در صورت مبتلا بودن جنین به اختلالات ژنتیکی نمی باشند.
روش آزمایشگاهی بسیار پیشرفته PGD که کمک می کند جنین ها بدون اختلال و نقص ژنتیکی متولد شود,آزمایش روی جنین هشت سلولی که حاصل لقاح مصنوعی (IVF یاICSI ) می باشد انجام می شود و تنها در صورت اطمینان از سالم بودن جنین,او را به رحم مادر منتقل می کنند.
به کارگیری روش PGD در فرآیند درمانی لقاح آزمایشگاهی IVF یا ICS باعث افزایش موفقیت تولد جنین سالم می شود زیرا قبل از مرحله لانه گزینی جنين از لحاظ ژنتیکی بررسی می شود و در صورت تایید سلامت انتخاب می شود.
بنابراین بواسطه این روش از تولد كودكانی با ناهنجاريهای ژنتيكی یا اختلالات کروموزمی که حتی ممکن است باعث سقط خود به خودی شود پیشگیری می شود.
علاوه بر این در روش PGD برای برداشتن سلول های جنينی (بلاستومر) جهت بررسی, به ناچار سوراخی در زونا پلاسیدا ايجاد می کنند كه اين مجرا می تواند باعث لانه گزينی بهتر جنين در رحم باشد (روش هچینگ).
مراحل انجام آزمایش PGD
یکی از مهم ترین اقدامات قبل از انجام PGD, شناسايی جهش ژنتيکی در والدين است. لازم است زوجين به خصوص آنهایی که احتمال بالایی برای انتقال ناهنجاریهای ژنتیکی دارند جهت ارزيابی ريسک انتقال اختلالات ژنتيکی به فرزندانشان حتما مشاوره شوند.
برای هر خانواده در یک مرحله 2-3 ماهه روی تک سلول آزمایش اختصاصی انجام می شود.پس از انجام این مرحله اعمال روش PGD از لحاظ ژنتیکی امکان پذیر می باشد.همانطور که گفته شد PGD به معنی نمونه برداری از جنین و ارسال یک سلول برای بررسی و تشخیص اختلال کروموزومی است که طی یک دوره لقاح مصنوعی (IVF یا ICSI) آغاز می شود و شامل تمامی مراحل این دو روش از جمله تحریک کردن تخمدان با دارو,تخمک گیری,لقاح در آزمایشگاه و در نهایت انتقال جنین به رحم مادر می باشد.
آزمایش PGD حدودا 48 ساعت زمان می برد و معمولا در روز سوم پس از لقاح در آزمایشگاه انجام می شود که حداقل 5 جنین ظاهرا سالم 6 تا 8 سلولی تشکیل شده باشد,در صورتی نتیجه آزمایش مشخص کند جنین سالم است عمل انتقال به رحم مادر انجام می شود.
در مراحل مختلف رشد جنینی میتوان از جنین نمونه برداری انجام داد.
در گذشته نه چندان دور نمونه برداری فقط از تخمک صورت می گرفت و در صورت سالم بودن تخمک آن را با اسپرم مرد لقاح می دادند و جنین حاصل را به رحم مادر منتقل می کردند.اما پس از تولد تعدادی نوزادانی با اختلال کروموزومی, امروزه نمونه برداری از جنین در روز سوم از رشد جنینی یعنی زمانیکه جنین 6 تا 8 سلولی استانجام می شود,یا در مواردی نمونه برداری در روز 5 تا 6 از رشد جنینی (بلاستوسیست) و یا مراحل پیشرفته تر رشد انجام می شود.
مراحل انجام PGD (تشخیص قبل از لانه گزینی)
1.کشت جنین تا روز سوم,جنین 6 تا 8 سلولی (بلاستوسیت)
2.برداشتن یک یا دو سلول از جنین (بلاستومر)
انجام PGD روی سلول های برداشته شده از طریق یکی از دو روش زیر:
- مولکولی
- سیتولوژیک
روش مولکولی:
کپی کردن DNA سلول از طریق فرآیندی به نام واکنش زنجیرهای (PCR) جهت تشخیص بیماری های تک ژنی.
روش سیتولوژیک:
آشکارسازی نواحی کروموزومی با استفاده از روش (FISH)
3.تحلیل مولکولی جهت ارزیابی کد دنباله DNA برای تعیین احتمال به ارث رسیدن یک ژن مشکل ساز.
4.انتقال جنین پس از انجام آزمایش PGD و شناسایی و انتخاب جنین های سالم
کاربرد روش PGD
برای هر زوجی که در معرض انتقال یک بیماری ژنتیکی می باشد انجام تشخیص پیش از لانه گزینی (PGD) ضروری است.
افراد مناسب برای آزمایش PGD
- مادران بالای 35 سال
لازم به ذکر است با افزایش سن مادر احتمال تولد نوزاد با سندرم داون حدود 10 برابر و سایر اختلالات کروموزومی 2 تا 3 برابر افزایش می یابد.
- زوجهایی که حداقل يکی از آنها مبتلا به بیماری ژنتیکی یا حامل آن باشد.
- یکی از زوجین حامل اختلالات ژنتیکی وابسته به جنس مانند هموفیلی باشد.
- یکی از زوجین حامل نقص ژن منفرد باشد مانند بیماری تک ژنی تالاسمی.
- یکی از طرفین اختلال کروموزومیداشته باشد و یا در خانواده سابقه تولد بچه ناقص یا عقب وجود داشته باشد.
- خانمهایی که تجربه سقط مکرر ناشی از ناهنجاری های کروموزومی دارند.
- زمانی كه در آزمایش کاریوتایپ ناهنجاری های ساختاری جابجایی قطعات كروموزومی مشاهده شود.
- بیماران ناباروری که تجربه چندین بار (بیش از 3 بار) IVF یا میکرواینجکشن ناموفق داشته اند.
- در زوجيني که به دلیل مشکل باروری از جانب آقا کانديد روش ICSI (تزريق اسپرم به داخل تخمک) هستند.
جهت مشاوره, هماهنگی و رزرو وقت میتوانید از طرق سایت
اقدام نمایید و یا با شماره تلفن های درج شده تماس حاصل فرمایید.
شماره واتساپ






1 Comment
[…] از با سابقهترین روشهای کمک بارو&… است. سیکل IVF به این […]